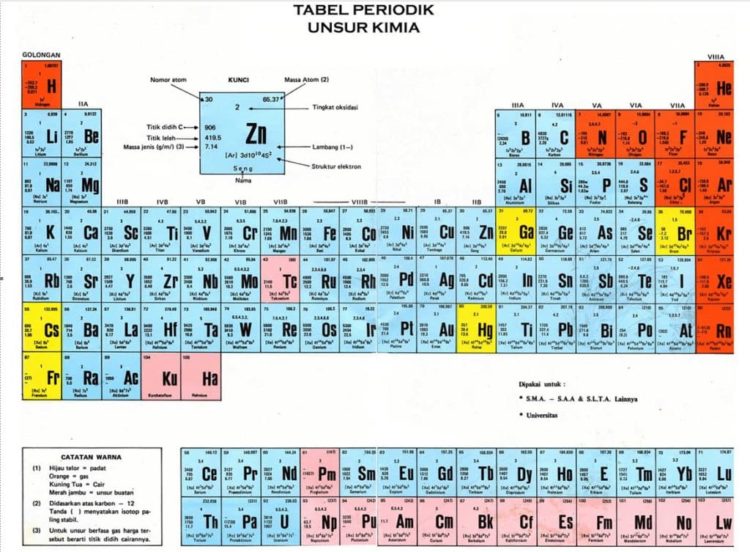
Tahukah kamu bahwa segala hal di dunia ini merupakan persatuan dari unsur-unsur kimia?
Semua unsur itu telah disusun oleh para ilmuwan menjadi tabel periodik.
118 unsur kimia pada tabel tersebut tersebar di seluruh dunia, mulai dari benda mati hingga makhluk hidup sekalipun.
Unsur tersebut merupakan bagian terkecil yang tidak bisa dibagi-bagi lagi.
Pengertian Tabel Periodik Unsur
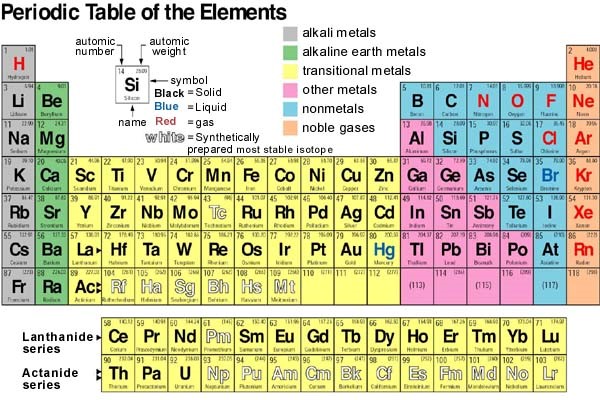
Tabel periodik unsur kimia merupakan sebuah wujud tabel yang menampilkan macam-macam unsur kimia.
Tabel tersebut disusun berdasarkan nomor atom atau banyaknya proton yang ada di dalam inti atom, konfigurasi dari elektron, serta sifat kimia dari unsur-unsur tersebut.
Tabel periodik dipetakan menjadi 4 blok yaitu –s, -p, -d, dan –f.
Kegunaan dari tabel periodik ini salah satunya yaitu sebagai penurunan sifat dari unsur kimia.
Selain itu, bisa juga untuk memprediksi sifat-sifat unsur kimia yang baru yang belum pernah ditemukan.
Tabel ini juga bisa menampilkan kerangka kerja untuk keperluan analisis di berbagai bidang, khususnya bidang kimia.
Dalam susunan tabel periodik, biasanya pada bagian kiri merupakan unsur logam, sebaliknya pada bagian kanan merupakan unsur non logam.
Bahkan, ada satu unsur yang memiliki sifat paling berbeda, yaitu uranium.
Uranium disebut sebagai unsur paling berat di alam semesta yang muncul secara alami.
Di Indonesia, uranium merupakan unsur kimia radioaktif yang jumlahnya cukup melimpah.
Selain itu, uranium juga berguna sebagai penambah berat pada kerangka kapal laut.
Sebelum kamu mempelajari lebih jauh tentang tabel periodik, kenali dulu beberapa istilah penting dalam pengelompokan unsur-unsur kimia, yaitu periode, golongan, dan blok.
Metode Pengelompokan
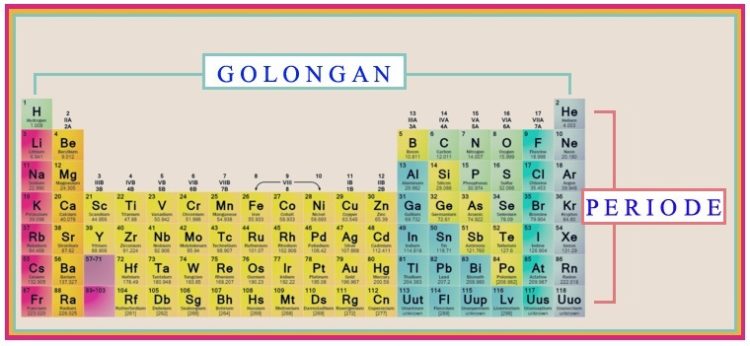
Golongan
Golongan adalah tampilan berupa kolom vertikal pada tabel periodik.
Ada sebanyak 6 golongan atau kolom yang memiliki nama sendiri selain nomor yang tercantum. Misalnya, unsur golongan 17 yaitu halogen, atau kolom 18 yakni gas mulia.
Kenaikan nomor atom dari masing-masing unsur juga bisa mempengaruhi kesamaan sifat dari unsur kimia yang bersangkutan.
Dalam teori mekanika kuantum modern menjelaskan bahwa, unsur kimia dalam kolom yang sama juga memiliki kesamaan dalam konfigurasi elektron pada bagian kulit valensinya.
Persamaan ini mengakibatkan unsur kimia yang berada pada satu kolom memiliki sifat yang jelas.
Namun pada bagian lain, kolom vertikal ini tidak berpengaruh pada persamaan sifat.
Secara Internasional, tatanama pada golongan ditandai dengan angka 1 sampai 18.
Penomoran dimulai dari kolom sebelah kiri yaitu logam alkali, sampai dengan kolom bagian kanan yaitu gas mulia.
Ada beberapa kolom yang memiliki susunan nama secara acak atau non sistematis.
Misalnya pada kolom 3-10, mereka tidak mempunyai nama trivial.
Penamaan pada kolom 3-10 hanya merujuk pada nama unsur dan nomor kolom teratas yang berada dalam satu baris kolom.
Unsur kimia yang tersusun dalam satu kolom, memiliki pola khusus pada jari-jari atom, elektronegativitas, dan energi ionisasinya.
Dalam satu golongan, jari-jari atom akan mengalami kenaikan dimulai dari urutan paling atas hingga paling bawah.
Periode
Periode adalah sebuah baris horizontal dalam tabel periodik. Ada bagian tertentu yang memiliki substansi khusus, misalnya pada blok –f.
Dalam baris blok itu, lantanida beserta aktinida akan bergabung dan membentuk dua seri berbentuk horizontal.
Dalam satu periode, unsur kimia akan menampilkan sifat dari segi jari-jari atom, afinitas elektron, energi ionisasi, serta elektronegativitas.
Jari-jari atom akan mengalami penyusutan dimulai dari unsur kimia sebelah kiri hingga ke kanan dalam satu baris periode.
Penyusutan ini terjadi karena adanya penambahan proton dan elektron pada unsur kimia yang berurutan.
Akibatnya, elektron tertarik mendekat menuju inti atom.
Selain itu, penyusutan jari-jari atom juga berpengaruh pada energi ionisasi.
Blok
Blok merupakan bagian dari tabel periodik yang berisi urutan unsur kimia berdasarkan kulit elektron.
Penamaan setiap blok juga didasari dengan subkulit yang menjadi tempat terakhir bagi elektron.
Nama-nama blok pada tabel periodik, yaitu:
Blok –s
Blok ini tersusun dari 2 kolom pertama yaitu alkali dan alkali tanah, keduanya bersifat logam.
Selain alkali dan alkali tanah, blok –s juga memiliki unsur kimia tambahan yakni hidrogen dan helium.
Blok –p
Pada blok ini tersusun atas 6 kolom terakhir, yakni kolom ke 13 sampai 18 (penamaan sesuai IUPAC). Di Amerika, kolom tersebut ditulis 3A sampai 8A.
Unsur kimia pada blok –p mengandung metaloid yang cukup besar.
Blok –d
Blok –d terdiri atas kolom ke 3 sampai 12, sedangkan di Amerika disebut kolom 3B sampai 2B.
Seluruh unsur di dalam blok –d merupakan logam transisi.
Blok –f
Blok ini sering berada pada bagian bawah tabel, karena tidak memiliki nomor golongan.
Unsur kimia yang tertera yaitu lantanida dan aktinida.
Permbagian Berdasarkan Sifat Fisika & Kimia
Unsur-unsur dalam tabel periodik dibagi menjadi 3 kategori berdasarkan sifat kimia dan sifat fisikanya.
3 kategori tersebut adalah:
Logam
Karakter logam secara umum yaitu memiliki kilau, konduktivitas tinggi dan padat.
Selain itu logam juga dapat berubah menjadi aloy bersama logam lainnya, serta dapat membentuk ion mirip garam dan non logam.
Secara rinci logam masuk dalam sub kategori dalam periode yang sama, urutan tersebut mengindikasikan perubahan sifat logam menuju non logam.
Logam juga dibagi menjadi beberapa unsur, yaitu alkali yang bersifat reaktif, alkali tanah yang bersifat kurang reaktif, lantanida beserta aktinida, serta logam transisi.
Unsur terakhir yaitu logam pasca-transisi yang bersifat sifat fisika dan kimia yang cenderung lemah.
Meskipun unsur kimia telah dikelompokkan berdasarkan kategori dan sub kategori sesuai kesamaan sifat, namun pembagian ini masih belum sepenuhnya sempurna.
Masih ada spektrum sifat di dalam masing-masing unsur.
Misalnya pada unsur berilium, unsur ini masuk dalam kategori logam alkali tanah.
Meskipun berilium lebih cenderung bersifat amfoter, namun ada reaksi kimia yang membuat berilium terlalu banyak membentuk senyawa kovalen.
Akibatnya, reaksi tersebut telah melemahkan posisi berilium sebagai logam.
Metaloid

Metaloid merupakan unsur yang memiliki sifat yang berada pada pertengahan logam dan non logam.
Selain itu, metaloid juga bisa memiliki sifat yang berasal dari campuran logam dan non logam.
Secara umum, metaloid bersifat semikonduktor pada aliran listrik dan permukaannya sedikit berkilau.
Contoh unsur metaloid di antaranya, boron (B), silikon (Si), germanium (Ge), arsen (As), antimon (Sb), telurium (Te), serta polonium (Po).
Susunan metaloid dalam tabel periodik diwujudkan dalam urutan yang membentuk garis diagonal, dimulai dari boron (B) sampai polonium (Po).
Non Logam
Dalam tabel periodik, unsur yang bersifat non logam sebagian besar terdiri dari gas berwarna maupun tidak berwarna.
Ada beberapa unsur non logam yang berubah bentuk menjadi senyawa bersama dengan unsur non logam lainnya, perubahan tersebut terikat secara kovalen.
Unsur non logam dapat dibagi menjadi:
- Non logam poliatomik dimana unsur tersebut mirip dengan metaloid.
- Non logam diatomik atau disebut juga non logam esensial
- Gas mulia monoatomik yang dikenal juga sebagai non logam dengan inert yang sempurna.
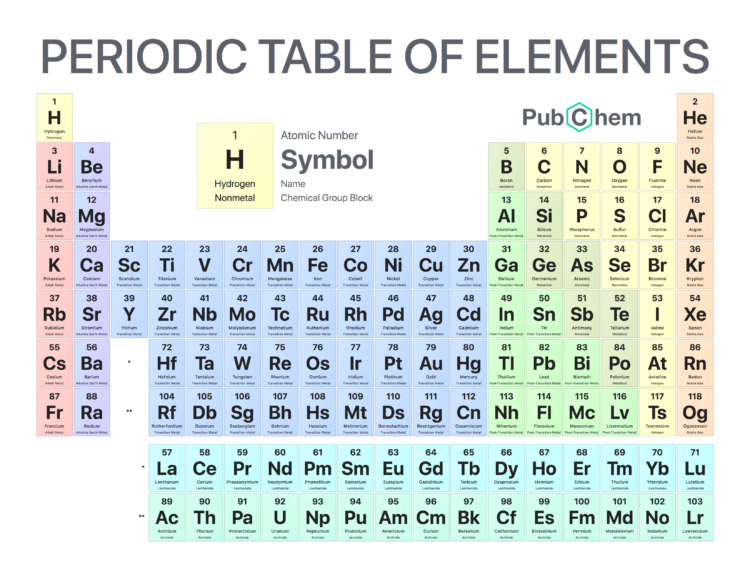
Tabel Periodik Unsur Lengkap
| No atom | Unsur Kimia | Simbol | No atom | Unsur Kimia | Simbol |
| 1 | hidrogen | H | 60 | neodymium | Nd |
| 2 | helium | He | 61 | promethium | Pm |
| 3 | lithium | Li | 62 | samarium | Sm |
| 4 | beryllium | Be | 63 | europium | Eu |
| 5 | boron | B | 64 | gadolinium | Gd |
| 6 | carbon | C | 65 | terbium | Tb |
| 7 | nitrogen | N | 66 | dysprosium | Dy |
| 8 | oxygen | O | 67 | holmium | Ho |
| 9 | fluorine | F | 68 | erbium | Er |
| 10 | neon | Ne | 69 | thulium | Tm |
| 11 | sodium | Na | 70 | ytterbium | Yb |
| 12 | magnesium | Mg | 71 | lutetium | Lu |
| 13 | aluminum | Al | 72 | hafnium | Hf |
| 14 | silicon | Si | 73 | tantalum | Ta |
| 15 | phosphorus | P | 74 | tungsten | W |
| 16 | sulfur | S | 75 | rhenium | Re |
| 17 | chlorine | Cl | 76 | osmium | Os |
| 18 | argon | Ar | 77 | iridium | Ir |
| 19 | potassium | K | 78 | platinum | Pt |
| 20 | calcium | Ca | 79 | gold | Au |
| 21 | scandium | Sc | 80 | mercury | Hg |
| 22 | titanium | Ti | 81 | thallium | Tl |
| 23 | vanadium | V | 82 | lead | Pb |
| 24 | chromium | Cr | 83 | bismuth | Bi |
| 25 | manganese | Mn | 84 | polonium | Po |
| 26 | iron | Fe | 85 | astatine | At |
| 27 | cobalt | Co | 86 | radon | Rn |
| 28 | nickel | Ni | 87 | francium | Fr |
| 29 | copper | Cu | 88 | radium | Ra |
| 30 | zinc | Zn | 89 | actinium | Ac |
| 31 | gallium | Ga | 90 | thorium | Th |
| 32 | germanium | Ge | 91 | protactinium | Pa |
| 33 | arsenic | As | 92 | uranium | U |
| 34 | selenium | Se | 93 | neptunium | Np |
| 35 | bromine | Br | 94 | plutonium | Pu |
| 36 | krypton | Kr | 95 | americium | Am |
| 37 | rubidium | Rb | 96 | curium | Cm |
| 38 | strontium | Sr | 97 | berkelium | Bk |
| 39 | yttrium | Y | 98 | californium | Cf |
| 40 | zirconium | Zr | 99 | einsteinium | Es |
| 41 | niobium | Nb | 100 | fermium | Fm |
| 42 | molybdenum | Mo | 101 | mendelevium | Md |
| 43 | technetium | Tc | 102 | nobelium | No |
| 44 | ruthenium | Ru | 103 | lawrencium | Lr |
| 45 | rhodium | Rh | 104 | rutherfordium | Rf |
| 46 | palladium | Pd | 105 | dubnium | Db |
| 47 | silver | Ag | 106 | seaborgium | Sg |
| 48 | cadmium | Cd | 107 | Bohrium | Bh |
| 49 | indium | In | 108 | Hassium | Hs |
| 50 | tin | Sn | 109 | meitnerium | Mt |
| 51 | antimony | Sb | 110 | Darmstadtium | Ds |
| 52 | tellurium | Te | 111 | Roentgenium | Rg |
| 53 | iodine | I | 112 | Copernicium | Cn |
| 54 | xenon | Xe | 113 | Ununtrium | Uut |
| 55 | cesium | Cs | 114 | Ununquadium | Uuq |
| 56 | barium | Ba | 115 | Ununpentium | Uup |
| 57 | lanthanum | La | 116 | Ununhexium | Uuh |
| 58 | cerium | Ce | 117 | Ununseptium | Uus |
| 59 | praseodymium | Pr | 118 | Ununoctium | Uuo |
Berikut ini adalah tabel periodik unsur secara lengkap.
Agar kamu bisa mempelajarinya lebih lama, silahkan download gambar tabel periodik terbaru di bawah ini:
Dalam mempelajari unsur kimia, kamu juga akan menemukan istilah-istilah penting lainnya, di antaranya:
Konfigurasi Elektron
Konfigurasi elektron dikenal juga sebagai sebuah organisasi dari elektron yang mengitari atom netral.
Putaran elektron tersebut memiliki pola yang berulang atau disebut juga periodisitas.
Elektron tersebut berada pada rangkaian kulit 1, kulit 2, kulit 3, dan seterusnya.
Dari masing-masing kulit tersebut memiliki subkulit yang berjumlah 1 atau lebih.
Subkulit elektron diberi nama s, p, d, f dan g.
Dengan pola peningkatan nomor pada atom, elektron akan memasuki bagian kulit serta subkulitnya, hal sesuai dengan teori dari Madelung.
Contohnya pada konfigurasi neon yakni 1s2 2s2 2p6 .
Dengan nomor atom berjumlah 10, neon memiliki 2 elektron di bagian kulit pertamanya, kemudian ada 8 elektron pad kulit keduanya.
8 elektron pada kulit kedua terbagi menjadi 2 elektron di subkulit s, dan 6 elektron pada subkulit p.
Pada tabel periodik, elektron yang pertama kali berada pada kulit baru berarti akan memulai periode baru. Dalam hal ini, unsur yang dimaksud adalah logam alkali dan hidrogen.
Jari-jari Atom
Jari-jari atom dalam tabel periodik ditampilkan secara variatif.
Misalnya pada satu periode, unsur kimia di dalamnya memiliki jari-jari atom yang disusun secara menurun, mulai dari jenis logam alkali sampai gas mulia.
Sementara jari-jari atom yang disusun meningkat, ditujukan untuk unsur kimia pada satu golongan mulai dari atas menuju bawah.
Jari-jari atom meningkat secara signifikan dari gas mulia yang terletak di akhir periode, sampai dengan logam alkali yang berada di awal periode selanjutnya.
Hal-hal yang menerangkan jari-jari atom ini telah dijelaskan melalui teori kulit elektron atom.
Teori tersebut kemudian berkembang menjadi Teori Kuantum.
Energi Ionisasi
Energi ionisasi pertama merupakan energi yang telah diserap oleh atom guna melepaskan 1 elektron.
Sedangkan energi ionisasi kedua adalah, untuk melepaskan elektron kedua, dan berlanjut pada elektron seterusnya.
Pada sebuah atom, energi ionisasi diurutkan secara meningkat setara dengan peningkatan derajat ionisasi.
Misalnya pada magnesium, energi ionisasi pertamanya adalah 738 kJ/mol, sedangkan energi ionisasi keduanya adalah 1.450 kJ/mol.
Dalam satu golongan, energi ionisasi akan meningkat mulai dari bawah ke atas.
Sementara dalam satu periode, energi ionisasi meningkat dimulai dari bagian kiri menuju kanan.
Energi ionisasi akan semakin besar pada saat terjadi pelepasan satu elektron dari sebuah konfigurasi pada gas mulia.
Contohnya unsur magnesium, energi ionisasi pertama (738 kJ/mol) dan kedua (1.450 kJ/mol) berguna untuk melepaskan 2 elektron 3s, sedangkan energi ionisasi ketiga jauh lebih besar yaitu 7.730 kj/mol.
Jika unsur kimia memiliki ikatan yang semakin kuat, maka energi yang dibutuhkan untuk melepaskan elektron juga semakin besar.
Dalam tabel periodik, urutan unsur kimia dari atas ke bawah memiliki urutan energi ionisasi yang menurun.
Hal ini disebabkan oleh ikatan atom yang lemah, sehingga elektron mudah lepas.
Elektronegativitas
Elektronegativitas merupakan kecenderungan sebuah atom dalam menarik elektron.
Elektronegativitas ini dipengaruhi oleh nomor atom serta jarak elektron valensi dengan bagian inti atom.
Semakin besar tingkat elektronegativitasnya, maka akan semakin besar juga kekuatan unsur kimia dalam menarik elektron.
Teori ini dinyatakan oleh Linus Pauling.
Elektronegativitas tersusun secara meningkat dalam tabel periodik, dimulai dari bagian kiri menuju kanan dalam satu periode.
Sedangkan dalam satu golongan, tersusun menurun mulai dari atas hingga ke bawah.
Berdasarkan teori ini, maka unsur yang paling elektronegatif adalah fluor.
Sedangkan unsur yang paling lemah elektronegativitasnya adalah sesium.
Namun ada beberapa pengecualian, yaitu pada unsur galium dan germanium.
Kedua unsur tersebut memiliki elektronegativitas lebih besar dibandingkan dengan aluminium dan silikon.
Hal ini terjadi akibat adanya kontraksi pada blok –d.
Selain itu, pengecualian lainnya adalah pada golongan 11, yaitu elektronegativitas mengalami kenaikan dari atas menuju bawah.
Afinitas Elektron
Afinitas elektron adalah sebuah istilah untuk menunjukkan jumlah energi yang telah dilepaskan oleh atom.
Pelepasan elektron ini terjadi saat elektron masuk menuju atom netral guna membentuk ion yang bersifat negatif.
Unsur kimia non logam memiliki afinitas elektron yang lebih positif dibandingkan dengan unsur logam.
Secara umum, afinitas elektron tersusun secara meningkat dalam satu periode.
Hal ini disebabkan adanya kulit valensi atom yang telah terisi penuh.
Misalnya, atom pada golongan 17 akan mengeluarkan energi yang lebih besar dibandingkan atom pada golongan 1.
Proses ini terjadi karena atom golongan 17 memiliki kulit valensi yang penuh dan stabil.
Afinitas elektron cenderung menurun sepanjang baris golongan, mulai dari atas menuju bawah.
Biasanya dalam satu golongan tersebut, beberapa unsur kimia dengan bobot lebih berat memiliki afinitas elektron yang lebih tinggi.
Sebaliknya, beberapa unsur yang berbobot ringan memiliki afinitas elektron yang rendah.
Pada baris periode, afinitas elektron ditunjukkan dengan urutan meningkat mulai dari kiri menuju kanan.
Pada bagian kiri tersusun atas unsur kimia logam, sedangkan bagian kanan terdiri dari unsur kimia non logam.
Namun, rumusan afinitas elektron ini tidak berlaku pada unsur gas mulia.
Cara Membaca Tabel Periodik
Gambar di bawah ini merupakan contoh potongan tabel periodik dan keterangan simbolnya:

Berdasarkan gambar di atas, cara membacanya adalah:
- Nomor atom ditunjukkan oleh angka 12.
- Lambang unsur kimia diwujudkan dalam wujud Mg.
- Nama unsur yaitu magnesium berada di bawah lambang unsur.
- Nomor massa ditulis berada paling bawah, yakni 24.035.
Maka jika dirangkum, unsur kimia magnesium (Mg) memiliki nomor atom 12, dan nomor massa 24.035.
Cara Menghapal Tabel
Tabel periodik berisi unsur-unsur kimia yang sangat banyak, masing-masing unsur memiliki lambang yang berbeda-beda.
Pertanyaan yang sering muncul, apakah benar tabel periodik itu susah untuk dihafal?
Jawabannya tentu tidak, asal kamu ada niat dan kemauan.
Kamu hanya membutuhkan trik khusus untuk bisa menghafalnya dengan cepat.
Bahkan, kamu juga bisa menggunakan istilah singkatan selain dari Bahasa Indonesia yang kamu anggap mudah, misalnya dengan bahasa Jawa, bahasa Sunda atau bahasa daerah lainnya.
Berikut merupakan cara menghafal tabel periodik berdasarkan baris golongan.
Golongan 1A H Alkali
H = Hidrogen, dibaca Ha
Li = Litium, dibaca Li
Na = Natrium, dibaca Na
K = Kalium, dibaca Kalah
Rb = Rubidium, dibaca Roni pun
Cs = Cesium, dibaca Cemas dan
Fr = Fransium, dibaca Frustasi
Maka, secara menyeluruh dibaca Halina kalah, Roni pun cemas dan frustasi.
Golongan 2A Be Alkali Tanah
Be = Berilium, dibaca Bebek
Mg = Magnesium, dibaca Mangan
Ca = Kalsium, dibaca Cacing
Sr = Stronsium, dibaca Seret
Ba = Barium, dibaca Banget
Ra = Radium, dibaca Rasane
Maka, rangkuman kalimatnya adalah bebek mangan cacing, seret banget rasane.
Golongan 3A B Boron atau Aluminium
B = Boron, dibaca Bang
Al = Aluminium, dibaca Ali dan
Ga = Galium, dibaca Galih
In = Indium, dibaca Injak
Tl = Titanium, dibaca Tali
Rangkaian kalimatnya adalah bang Ali dan Galih injak tali.
Golongan 4A C Karbon
C = Carbon, dibaca Cewek
Si = Silikon, dibaca Seksi
Ge = Germanium, dibaca Gandeng
Sn = Stannum, dibaca Seorang
Pb = Plumbum, dibaca Pria
Tersusun menjadi, cewek seksi gandeng seorang pria.
Golongan 5A N Nitrogen
N = Nitrogen, dibaca Nembak
P = Phosphorus, dibaca Perempuan
As = Arsenik, dibaca Asal
Sb = Stibium, dibaca Sabar pasti
Bi = Bismut, dibaca Bisa
Susunan kata-kata tersebut menjadi nembak perempuan asal sabar pasti bisa.
Golongan 6A O Oksigen
O = Oksigen, dibaca Om
S = Sulfur, dibaca Satria
Se = Selenium, dibaca Sedang
Te = Telurium, dibaca Telepon
Po = Polonium, dibaca Polisi
Gabungan kata-kata tersebut menjadi Om Satria sedang telepon Polisi.
Golongan 7A Fluron
F = Fluorin, dibaca Farhan
Cl = Klorin, dibaca Culun
Br = Bromin, dibaca Baru
I = Iodin, dibaca Ikut lomba
At =Astatin, dibaca Atletik
Kata-kata tersebut disusun menjadi Farhan culun baru ikut lomba atletik.
Golongan 8A Helium
He = Helium, dibaca Hebohnya
Ne = Neon, dibaca Negara
Ar = Argon, dibaca Arab
Kr = Kripton, dibaca Karena
Xe = Xenon, dibaca Xenit
Rn = Radon, dibaca Runtuh
Rangkuman kalimatnya menjadi hebohnya negara Arab karena xenit runtuh.
Sejarah Tabel Periodik Unsur

Susunan tabel periodik tidak lepas dari sejarah panjang dari para ilmuwan, bahkan tabel ini terbentuk dari beberapa percobaan yang mengalami perubahan setiap masanya.
Berikut sejarah pembentukan tabel periodik secara lengkap:
Tahun 1789
Antonie Lavoisier menerbitkan unsur kimia sebanyak 33 daftar.
ntonie menyusunnya berdasarkan kategori gas, tanah, logam, serta non logam.
Setelah itu para ilmuwan kimia terus berusaha menciptakan skema klasifikasi yang lebih jelas dan memadai.
Penelitian tersebut bahkan berlangsung hampir 1 abad.
Tahun 1829
Johann Wolfgang Döbereiner menyatakan bahwa unsur-unsur kimia bisa dikelompokkan dalam triad.
Pengelompokkan tersebut disesuaikan dengan sifat kimia dari masing-masing unsur. Misalnya unsur litium, natrium, serta kalium.
Mereka disatukan dalam triad karena memiliki persamaan yakni logam lunak dan bersifat reaktif.
Johann juga berpendapat bahwa, apabila susunan unsur kimia didasarkan pada berat atom, maka anggota triad yang kedua akan memiliki berat atom yang setara dengan rata-rata berat atom anggota pertama dan ketiga.
Teori ini kemudian dikenal dengan Hukum Triad.
Tahun 1843
Leopold Gmelin yang merupakan ilmuwan kimia dari Jerman, melakukan penelitian pada Hukum Triad.
Penelitiannya dilakukan dengan cara mengidentifikasi 10 triad.
Leopold membaginya menjadi 3 kelompok empat, serta 1 kelompok lima.
Tahun 1857
Jean Baptiste Dumas menerbitkan hasil penelitiannya pada tahun ini.
Penelitian tersebut menjelaskan adanya hubungan di dalam kelompok logam.
Meskipun Jean dibantu oleh banyak ilmuwan kimia, namun identifikasi hubungan antar kelompok dari unsur kimia masih belum diwujudkan dalam skema yang memadai.
Tahun 1858
Pada tahun ini, ilmuwan kimia bernama August Kekulé melakukan sebuah pengamatan pada karbon.
Dari hasil pengamatan tersebut, diketahui bahwa karbon sering menarik karbon lainnya sebanyak 4 buah.
Contohnya pada metana, unsur ini memiliki 1 atom karbon dan 4 atom hidrogen.
Pengamatan ini kemudian dikenal sebagai teori valensi, yaitu adanya unsur kimia yang terikat dengan beberapa atom yang berbeda.
Tahun 1862
Alexandre-Emile Béguyer de Chancourtois, seorang geolog dari Prancis mulai mengenalkan kepada publik tentang tabel periodik, yaitu telluric helix (sekrup).
Ilmuwan inilah yang pertama kali menuliskan tentang periodisitas unsur kimia.
Unsur tersebut disusun dengan bentuk spiral pada sebuah silinder, urutannya disesuaikan dengan kenaikan berat pada atom.
Pada tabel telluric helix tidak hanya tertera nama unsurnya saja, namun juga terdapat ion dan senyawa tambahan lainnya.
Teori dari Alexandre-Emile Béguyer de Chancourtois lebih sering menggunakan istilah geolog, dan tidak terdapat gambar.
Akibatnya, tidak banyak orang yang tertarik sampai akhirnya teori tersebut dilanjutkan oleh Dmitri Mendeleev.
Tahun 1864
Seorang ilmuwan kimia asal Jerman yakni Julius Lothar Meyer, mulai mengumumkan sebuah tabel yang memuat 44 unsur kimia.
Unsur-unsur tersebut disusun sesuai dengan valensinya, serta menampilkan beberapa persamaan sifat yang dimiliki.
Menurut Julius, unsur kimia yang memiliki sifat yang sama, juga memiliki valensi yang sama.
Selain Julius, ada juga ilmuwan lain yang mengumumkan tabel unsur kimia, yaitu William Odling.
Tabel yang dipublikasikan berisi 57 unsur kimia yang diurutkan berdasarkan berat dari masing-masing atom.
Pada tahun 1870, William memperbarui tabelnya dengan merubah klasifikasi unsur kimianya.
Perubahan tersebut didasarkan pada valensi dari setiap unsur.
Tahun 1863 – 1866
John Newlands dari Inggris, secara berkala menerbitkan makalah mulai tahun 1863 sampai 1866.
Makalah tersebut menuliskan pembahasan bahwa jika unsur kimia disusun berdasarkan kenaikan berat atomnya, maka sifat fisika dan kimianya akan terulang setelah sampai interval ke-8.
Karena mirip dengan susunan oktaf musik, maka teori ini dikenal sebagai Hukum Oktaf.
Selain Hukum Oktaf, John Newlands juga menciptakan tabel unsur kimia.
Tabel tersebut digunakan untuk memprediksi eksistensi unsur kimia yang belum ditemukan, misalnya germanium.
Pemikiran ini telah diakui oleh Chemical Society setelah 5 tahun sebelumnya mengakui teori dari Mendeleev.
Tahun 1867
Gustavus Hinrichs dari Amerika mulai menulis penemuannya di tahun ini.
Hinrichs menyatakan bahwa unsur kimia dapat digambarkan melalui garis batas yang sederhana.
Garis tersebut kemudian membentuk tabel periodik dengan menampilkan urutan unsur-unsur kimia.
Sistem periodik tersebut disusun secara spiral dengan landasan dasar urutan spektrum atom dan berat atom.
Tidak hanya itu, susunan tersebut juga disesuaikan dengan persamaan sifatnya, misalnya logam, non logam, dan gas.
Tahun 1869
Dari sekian banyak ilmuwan yang telah melakukan penelitian, namun hanya teori Dmitri Mendeleev yang paling populer, karena menampilkan tabel periodik lengkap.
Banyak pihak yang mengakui teori Mendeleev karena banyak prediksi yang akhirnya terbukti kebenarannya.
Tabel periodiknya disusun sesuai sifat-sifat unsur kimia yang telah diketahui.
Tidak hanya itu, Mendeleev juga memberikan tempat kosong untuk unsur-unsur yang belum diketahui identitasnya secara detail.
Kesimpulan
Ilmu kimia memang terlihat susah karena memiliki banyak teori yang sangat kompleks. Tetapi bukan berarti tidak bisa untuk dipelajari, ya.
Karena kenyataannya, ilmu kimia memiliki banyak manfaat dalam kehidupan manusia.
Tabel periodik hanyalah materi dasar sebelum melanjutkan ke pembahasan teori kimia lainnya yang lebih rinci.